מדעני מכון ויצמן למדע למחקר זיהו היום (שני) לראשונה את התאים שאחראים על אחת מפעולות החיים הבסיסיות ביותר – ייצור הורמון הנותן פקודה לייצר תאי דם אדומים. הממצאים צפויים לפרוץ דרך לטיפולים רפואיים חדשניים במצבים שונים של אנמיה.
ההורמון החשוב הזה אמנם זוהה כבר לפני עשרות שנים, אולם עד היום לא היה ידוע באילו תאים בגוף הוא מיוצר. במחקר חדש המתפרסם בכתב-העת המדעי Nature Medicine, זיהו מדענים מקבוצת המחקר של פרופ' עידו עמית במכון ויצמן למדע ועמיתיהם למחקר בישראל, באירופה ובארה"ב תת-קבוצה נדירה של תאי כליה, וחשפו כי תאים אלה הם היצרנים העיקריים של ההורמון בגוף האדם.
למעשה, התאים שלנו זקוקים לחמצן כמו אוויר לנשימה. כדי לספק להם צורך חיוני זה, הגוף שלנו מייצר בכל שנייה כ-3-2 מיליון כדוריות דם אדומות, כרבע מכלל התאים החדשים שנוצרים בגוף בכל רגע נתון. תהליך זה מוכתב על-ידי הורמון שנקרא אריתרופויאטין (או בקיצור EPO) שתפקידו להיקשר לתאי האב של כדוריות הדם הנמצאים בלשד העצמות ולגרום להם להתחלק ולהתרבות.
שלא בטובתו, EPO התפרסם בציבור בעיקר בשל ניצולו לרעה על-ידי ספורטאים. הדוגמא המוכרת ביותר לכך היא רוכב האופניים לאנס ארמסטרונג, אשר השתמש בגרסה סינתטית של ההורמון כדי לשפר את הסיבולת שלו בדרך לשבעה ניצחונות רצופים ב"טור דה פראנס". ואולם הפוטנציאל הטיפולי העצום הטמון בהורמון זה גדול ורחב בהרבה מהשימוש בו כסם משפר ביצועים.
נכון להיום, יותר מ-10% מהאוכלוסייה בעולם המערבי סובלים ממחלות כליה כרוניות, שמובילות בלא מעט מהמקרים לפגיעה בייצור ה-EPO ולאנמיה שעלולה להיות מסכנת חיים. עד לאחרונה, הדרך היחידה לטפל בסוג זה של אנמיה הייתה שימוש ב-EPO שהונדס במעבדה במטרה לפצות על החסך בהורמון הטבעי.
בשנים האחרונות, בעקבות ממצאים חדשים על תגובת תאי הגוף למצבים של מחסור בחמצן (היפוקסיה) – ממצאים שאף זיכו את המדענים שגילו אותם בפרס נובל לרפואה לשנת 2019 – פותחו כמה תרופות להגברת הייצור של EPO; אחת מהן זכתה באחרונה לאישור של מנהל המזון והתרופות האמריקאי (FDA). ואולם, אף שתרופה זו הוכחה כיעילה ובטוחה, הפיתוח שלה – ושל התרופות האחרות – נעשה מבלי לדעת את זהות התאים יצרני ה-EPO שעליהם הן אמורות להשפיע.
"גילוי תאי הנורן יאפשר כעת להבין כיצד תרופות אלה פועלות וחשוב מכך – יאפשר לפתח תרופות וטיפולים חדשים", אמר פרופ' עמית ומזכיר כיצד גילוי תאי בטא, יצרני האינסולין בלבלב, בשנות ה-50 של המאה הקודמות סלל את הדרך לטיפולים חדשים במחלת הסוכרת. "בטווח הארוך יותר, עשויות להתפתח גישות טיפוליות חדשות שיאפשרו להפעיל מחדש את תאי הנורן או לחדש את אוכלוסייתם, בדומה לטיפולים פורצי הדרך שפותחו באחרונה למחלת הסוכרת וכוללים השבה של תאי בטא תקינים ללבלב של חולים", הוסיף.
קיצור תולדות ה-EPO
הראשון לתעד את הקשר בין זמינות חמצן בסביבה לייצור תאי דם אדומים היה הרופא והחוקר הצרפתי פרנסואה ויול, שהבחין במהלך מסעותיו בפרו בסוף המאה ה-19 כי הדם שלו ושל עמיתיו נעשה סמיך יותר לאחר שנדדו מעיר הבירה לימה הנמצאת בגובה פני הים, לאזור הררי ודליל בחמצן הנמצא בגובה 4,200 מטר.
כשני עשורים מאוחר יותר, בתחילת המאה ה-20, שני חוקרים צרפתים נוספים, פול קרנו וקלוטילד-קמי דה-פלנדר, העלו לראשונה את ההשערה שייצור תאי הדם האדומים מווסת על-ידי גורמים בנוזלי הגוף, מה שלימים יכונה המערכת ההורמונאלית, אך רק בשנות ה-70 של אותה מאה – ולאחר 15 שנים של ניסיונות – הצליח הביוכימאי האמריקאי יוג'ין גולדווסר לבודד את מולקולת ה-EPO האנושי.
בכך סלל גולדווסר את הדרך לייצורו הסינתטי של EPO ולשימוש בו כתרופה מצילת חיים לחולי אנמיה (ודרך בלתי חוקית לספורטאים לשפר את ביצועיהם). בהמשך זוהה גם הגן המקודד ל-EPO והונחו היסודות לתגליותיהם של חתני פרס נובל לשנת 2019, וויליאם קיילין, פיטר רטקליף וגרג סמנזה, שחשפו כיצד תאים מסתגלים לשינויים ברמות החמצן.

ההורמון החמקמק
בניגוד לאינסולין או הורמונים חיוניים אחרים, EPO אינו נאגר בתאים, אלא מיוצר ומשתחרר במהירות בתגובה למחסור בחמצן. "היקף הייצור התאי שלו מזנק או צונח בחדות ובמהירות – ולכן זיהוי התאים המייצרים אותו מאתגר כל כך", מסביר פרופ' רולנד ונגר מאוניברסיטת ציריך, שחוקר את תהליך הייצור של EPO ב-30 השנים האחרונות והיה שותף מרכזי במחקר הנוכחי. "במשך עשרות שנים, זהותם של יצרני ה-EPO הייתה שנויה במחלוקת. אפשר לומר שכמעט כל תא בכליות נחשד בשלב זה או אחר כיצרן של הורמון זה", הוסיף.
קבוצת המחקר של פרופ' ונגר עשתה כברת דרך משמעותית בדרך לזיהוי התאים. במחקרים קודמים, הם יצרו באמצעות הנדסה גנטית עכברים שבהם התאים אשר מייצרים EPO זורחים באור פלואורסצנטי אדום. מחקר זה הצליח למקד את החוקרים באזור הספציפי בכליות שבו שוכנים יצרני ה-EPO ולחשוף שמדובר בתת-סוג של פיברובלסטים – תאים האחראים על ייצורה של רקמת החיבור של הגוף. עם זאת, זהותם המדויקת של התאים נותרה בגדר תעלומה.
כעת, בעזרת טכנולוגיות ניתוח מתקדמות ברמת התא הבודד שפותחו במעבדתו של פרופ' עמית ומאפשרות לחקור עשרות אלפי תאים בודדים בו-זמנית ולזהות סוגי תאים נדירים ברקמות, הצליחו במחקר החדש לחשוף לראשונה את זהות התאים החמקמקים.
ואולם, גם עם השיטות המתקדמות של פרופ' עמית והעכברים המהונדסים של פרופ' ונגר, זיהוי התאים היה אתגר לא פשוט. "לתאים הללו אין סמנים ידועים, בתנאי חמצן רגילים הם מייצרים כמות מזערית של EPO – ובתנאי מחסור בחמצן, ייצור ההורמון אינו סדיר", מסבירה את הקשיים ד"ר ביורט קרגסטין.
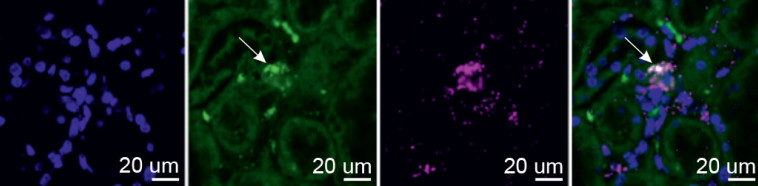
רק לאחר ניסיונות חוזרים ונשנים ובתנאי מחסור בחמצן, הצליחו החוקרים לזהות לבסוף מבין כ-3,000 תאי כליה שזרחו באדום בעכברים המהונדסים פחות מ-40 תאים אשר מייצרים EPO באופן פעיל. החוקרים אף פענחו את הדפוס המולקולרי של תאים אלה והראו כי גם בתנאי חמצן רגילים אלו אותם תאים אשר מייצרים את ה-EPO.
"האתגר הבא שלנו היה לאתר את התאים האלה בבני-אדם. המפתח לגילוי זה היה בהשגת דגימות כליה שהוצאו מאנשים שמתו כתוצאה ממחסור בחמצן", אומרת ד"ר קרגסטין. בסיועו של פרופ' ונגר יצרו החוקרים קשר עם מדען פורנזי גרמני שברשותו מאגר תרומות כליה של נפגעי שריפות שמתו מהרעלת פחמן חד-חמצני. דגימות אלו אפשרו לחוקרים לזהות את תאי הנורן גם בבני-אדם ולהראות שמדובר באותם התאים שזוהו בעכברים.
ד"ר ברק רוזנצוויג, אונקולוג אורולוגי בכיר במרכז הרפואי שיבא שהשתתף במחקר, אמר: "חולי סרטן רבים מקבלים כיום עירוי דם לפני ניתוחים כדי לשפר את ספירת תאי הדם האדומים שלהם. עירויים אלו עלולים להשפיע לרעה על המערכת החיסונית שלהם ולפגוע ביכולתם להילחם בסרטן בטווח הארוך", הוא מסביר. "הממצאים החדשים עשויים לאפשר פיתוח שיטות לעורר את התאים יצרני ה-EPO לפעולה ולשפר את ספירת הדם של המטופלים מבלי לפגוע במערכת החיסונית שלהם".
במחקר השתתפו גם תלמידת המחקר שחר הלוי ממעבדתו של פרופ' עמית, הגנטיקאי פרופ' יוזף פרצ'אל מאוניברסיטת יוטה ופרופ' אסקה וילרסלב ופרופ' פרננדו ראצימו מאוניברסיטת קופנהגן.

